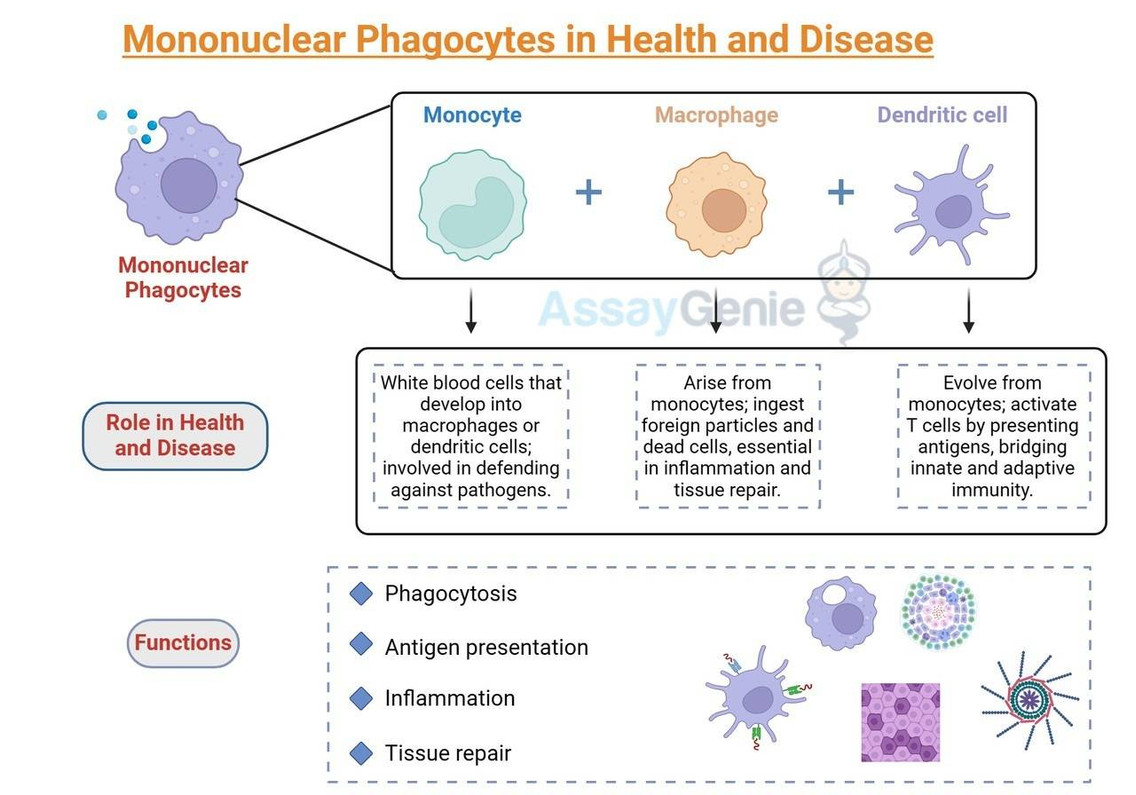
건강과 질병의 단핵 식세포
면역과 항상성에 필수적인 단핵 식세포는 식균 작용부터 조직 복구까지 다양한 역할을 수행하여 건강과 질병에 영향을 미칩니다.
주요 시사점:
단핵구, 대식세포, 수지상 세포를 포함한 단핵 식세포는 면역 방어와 생리학적 항상성에 중추적인 역할을 합니다.
기능은 식세포작용과 항원 제시에서부터 염증과 조직 복구에 이르기까지 다양합니다.
그들의 역할과 행동은 건강과 질병에 따라 다양하며 치료 목표에 대한 의미도 있습니다.
식세포란 무엇입니까?
혹시 한 곳을 짜서 흰 고름이 무엇인지 궁금해하신 적이 있습니까? 아니면 문신 뒤에 숨은 과학에 대해 의문을 품은 적이 있나요?
반점 발진은 면역 세포가 항상성을 회복하기 위해 면역 기능을 수행하는 감염 또는 부상 부위로 이동하는 염증 반응입니다. 마찬가지로, 1882년에 러시아 과학자 엘리 메치니코프(Elie Metchnikoff)는 불가사리에 장미 가시를 찔러서 세포가 장미 가시를 향해 이동하여 이를 삼키려고 시도하는 것을 관찰했습니다. 식세포작용 이론을 처음으로 생각해낸 것이 바로 이 실험이었습니다. 식균 작용은 주로 전문 식세포, 즉 과립구 및 단핵 식세포에 의해 수행되는 이물질을 삼키는 과정입니다.
식세포의 동정 이후, 이들 세포의 기원에 대한 관심이 생기기 시작했습니다. 초기 연구에서는 혈액 단핵구가 대식세포로 분화하는 능력이 입증되었습니다(Ebert and Florey, 1939). 이러한 연구를 통해 당시 과학자들은 순환 단핵구가 대부분의 조직 단핵구에 대한 전구 세포라는 결론을 내릴 수 있었습니다(van Furth et al., 1972).
1970년대에는 수상돌기로 인해 '별 모양' 형태를 갖는 새로운 세포 유형이 확인되었으며 이를 '수지상 세포'라고 불렀습니다. 오늘날 단핵구, 대식세포 및 수지상 세포는 면역 체계의 단핵 식세포로 통칭됩니다. 이 기사에서는 꾸준한 생리학적 조건과 염증 하에서 이들 세포가 수행하는 역할에 대해 논의할 것입니다.
단핵 식세포 시스템의 세포
인간 사이토카인
인간 사이토카인
사이토카인 ELISA 키트
고감도 사이토카인 ELISA 키트
마우스 사이토카인 ELISA 키트
대식세포
위에서 언급했듯이 대식세포는 몸 전체에 흩어져 있기 때문에 감염에 대한 최초 대응자가 되는 경우가 많습니다. 비록 모든 조직 내에서 발견되지만 서로 동일한 방식으로 행동하지는 않습니다. 대신 한 조직의 대식세포는 기능적으로나 전사적으로 다른 조직과 구별됩니다(Lavin et al., 2014).
대식세포 발달
단핵구는 조직 상주 대식세포의 전구체 세포로 간주되었지만, 1970년대 초반의 연구에서는 단핵구가 발생하기 전에 원시 대식세포가 난황낭 내에서 관찰되었기 때문에 이 이론에 도전했습니다(Cline and Moore, 1972; Takahashi, 1989). 최근에는 기술의 발전으로 대식세포 생물학자들이 대식세포의 기원을 진정으로 이해할 수 있게 되었습니다. 이제 대부분의 대식세포가 배아 발달 중에 파종된다는 것이 분명해졌습니다(Ginhoux et al., 2010; Schulz et al., 2012; Hashimoto et al., 2013; Yona et al., 2013; Epelman et al., 2014) 이는 정상 상태에서 단핵구와 독립적으로 성인기 전반에 걸쳐 자가 재생이 가능합니다(Soucie et al., 2016). 문신의 지속성은 조직에 상주하는 대식세포의 수명에 달려 있다고 믿어집니다.
조혈은 처음에는 원시 조혈로 알려진 난황낭에서 시작되며, 발달의 후기 단계에서는 태아의 간이 최종 조혈의 시작을 표시하는 주요 부위가 됩니다. 주목할 만한 점은 출생 시에 골수가 주요 부위가 된다는 것입니다. 결과적으로 조혈 세포는 이 세 가지 출처 중 어느 곳에서나 유래될 수 있습니다. 대식세포는 난황낭이나 태아간 유래 또는 둘의 조합입니다. 뇌의 미세아교세포는 난황낭 유래 대식세포의 대표적인 예인 반면(Ginhoux et al., 2010), 폐포 대식세포는 태아 간 기원(van de Laar et al., 2016)과 이중 기원의 랑게르한스 세포(Hoeffel 외., 2012). 이는 서로 다른 기원의 대식세포가 한 조직에서는 지배하고 다른 조직에서는 지배하지 않는 이유에 대한 의문을 제기합니다. 이 질문에 대한 답은 아직 알려지지 않았지만, 폐포 대식세포에 대한 예비 연구에서는 태아 간 대식세포가 GM-CSF를 통한 증식에 대한 반응 증가로 인해 폐포 틈새에서 난황낭 유래 대식세포를 능가하는 것으로 나타났습니다(van de Laar et al., 2016). 폐포 대식세포 발달에 필수적인 사이토카인입니다(Guilliams et al., 2013). 이는 세포 간의 경쟁이 발생하여 최근 Guilliams 그룹이 제안한 조직 틈새(tissue niche) 내에 더 적응된 세포가 존재하게 된다는 것을 의미합니다(Guilliams and Scott, 2017).
일반적인 합의는 조직 대식세포가 배아 기원이라는 것입니다. 그러나 과학 연구에는 항상 예외가 있습니다. 발달 후, 일부 조직의 대식세포는 자가 재생에 실패하며, 그 결과 순환하는 단핵구가 성인기 전반에 걸쳐 빈 틈새를 보충합니다(Bain et al., 2014; McGovern et al., 2014; Keller et al., 2017). 배아 대식세포 집단이 자가 재생에 실패하는 이유는 계속해서 조사되고 있습니다.
마르코파지와 혈관신생
대식세포는 기관 형성과 거의 동시에 파종되므로(Mass et al., 2016), 이들이 배아 발달 과정에서 역할을 하는지 의문이 듭니다. 실제로 소교세포가 결여된 쥐는 신경학적 장애에 기여하는 것으로 생각되는 감소된 시냅스 가지치기를 나타내는 것으로 관찰되었습니다(Paolicelli et al., 2011; Parkhurst et al., 2013). 마찬가지로, 심장 대식세포는 혈관 발달에 역할을 하는 것으로 알려져 있습니다(Leid et al., 2016).
발달 역할 외에도 대식세포는 성인기 동안 계속해서 항상성 역할을 수행합니다. 예를 들어 폐포 대식세포는 계면활성제 제거에 중요한 반면(van de Laar et al., 2016) 비장 대식세포는 철 항상성에 중요합니다(Kohyama et al., 2009). 대식세포는 단순히 '면역' 세포로 간주되기 때문에 우리가 흔히 당연하게 여기는 비면역 기능을 매일 조용히 수행합니다.
대식세포의 염증 역할
한 때 생각되었던 단핵구-대식세포 전구체 관계는 이후 개정되었으며 이제 이 분야의 과학자들은 두 세포가 서로 다른 세포 유형임을 시각화합니다. 염증의 맥락에서, 침윤하는 단핵구 유래 세포와 상주 대식세포는 부상/염증 부위에서 명백하지만, 이 두 집단은 여러 세포 표면 마커를 공유하기 때문에 시각적으로나 표현형적으로 해부하는 것이 어려울 수 있습니다. 연구에서는 두 집단을 구별하기 시작했으며 염증에 반응하여 선의의 상주 대식세포 집단의 역할을 조사하기 시작했습니다.
일부 연구에서는 상주 대식세포가 염증에 역할을 하지 않는 것으로 나타났습니다. 다발성 경화증 모델에서 단핵구 유래 세포는 염증 유발 유전자를 발현하는 반면, 소교세포의 프로필은 상대적으로 변하지 않습니다(Yamasaki et al., 2014). 다른 연구에서는 대식세포 소멸 반응(Barth et al., 1995)으로 지칭되는 손상 후 대식세포 수의 감소를 발견했습니다. 이 대식세포에 무슨 일이 일어나는지는 아직 불분명합니다. 반면, 상주 대식세포는 특정 염증 조건, 즉 Th2 반응에서 반응합니다. 이 환경에서는 단핵구 모집이 관찰되지 않으며 오히려 대식세포가 기생충 감염에 반응하여 증식하는 것으로 나타났습니다(Jenkins et al., 2011; Minutti et al., 2017).
종합적으로, 이들 연구는 생리적 조건과 염증 하에서 대식세포의 역할을 강조합니다.
수지상 세포
1970년대에 수지상 세포(DC)가 발견된 후(Steinman and Cohn, 1973), 이들 세포가 항원을 제시하고 순수 T 세포를 활성화하는 데 특화되어 있다는 것이 곧 밝혀졌습니다(Nussenzweig et al., 1980). 대식세포와 마찬가지로, 본질적으로 기존/고전적 DC(cDC) 또는 형질세포성 DC(pDC)로 분류될 수 있는 다양한 종류의 DC가 존재합니다. 흥미롭게도 두 가지 유형의 cDC가 마우스와 인간 모두에서 cDC1과 cDC2로 확인되었습니다. 최근 단일 세포 시퀀싱을 통해 추가로 새로운 하위 집합과 순환 전구체가 설명된 이러한 세포에 대한 더 깊은 탐색이 가능해졌으나(참조 et al., 2017; Villani et al., 2017), 여기서는 더 이상 논의하지 않습니다. 대식세포와 마찬가지로 DC도 고유한 계통을 지닌 단핵구와 독립적으로 유지됩니다.
최고의 ELISA 키트
pDC 기능
pDC는 림프구 활성화에 필요한 바이러스 자극에 반응하여 1형 인터페론을 생산하는 것으로 가장 잘 알려져 있습니다. pDC가 결핍된 마우스는 증가된 바이러스 부하와 낮은 수준의 1형 인터페론을 나타냅니다. pDC의 중요성은 이러한 세포가 부족하고 pDC 발달에 필요한 전사 인자(E2-2)의 돌연변이로 인해 바이러스 자극에 대한 반응을 유도할 수 없는 피트-홉킨스 증후군을 앓고 있는 인간 환자에서 입증되었습니다(Cisse et al. al., 2008).
cDC 기능
이름에서 알 수 있듯이 고전적인 DC는 항원 제시에 관여합니다. 이들 세포는 cDC가 결여된 마우스에서 입증된 바와 같이 T 세포 자극에 필요합니다(Jung et al., 2002). 외인성 항원과 내인성 항원 모두 제시될 수 있지만 cDC1 하위 집합은 cDC2보다 교차 제시에서 더 효율적입니다(den Haan, Lehar 및 Bevan, 2000; Bedoui et al., 2009).
단핵구 기능
단핵구는 한때 조직 대식세포와 수지상 세포를 채우는 순환 전구체로 간주되었습니다. 그러나 이제 대부분의 대식세포와 수지상 세포가 정상 상태에서 단핵구와 독립적으로 유지된다는 것이 분명해졌습니다. 결과적으로 이것은 단핵구의 진정한 기능이 무엇인가라는 질문을 제기합니다.
단핵구는 여러 종에 걸쳐 여러 하위 집합으로 구성된 이질적인 개체군입니다(Ziegler-Heitbrock, 2014). 인간의 경우, 순환 단핵구 풀의 약 80~90%를 구성하는 고전적 단핵구와 중간 및 비고전적 단핵구로 나머지를 구성하는 세 가지 하위 집합의 단핵구가 존재합니다. 최근 인간화 마우스를 사용하여 고전적 단핵구가 비고전적 단핵구로 성숙하는 경우 세 가지 하위 집합이 발달과 관련이 있는 것으로 나타났으며(Patel et al., 2017), 이는 마우스에서 유사한 결과를 반영합니다(Varol et al., 2007; Yona et al. , 2013; Gamrekelashvili 외, 2016; Mildner 외, 2017).
정상 상태 기능
고전적인 단핵구는 위에서 언급한 것처럼 배아 대식세포가 성인기 내내 지속되지 않는 조직 풀을 다시 채우는 것으로 알려져 있습니다(Bain et al., 2014; Epelman et al., 2014; McGovern et al., 2014; Keller et al., 2017). 또한 그들은 조직에서 림프절로 항원을 조사하고 운반하는 혈액 단핵구 특징을 유지하면서 조직에 들어가는 것으로 나타났습니다(Jakubzick et al., 2013). 반면, 비고전적 단핵구는 모든 손상을 모니터링하는 '하우스키퍼' 역할을 하며 내피를 순찰하는 정상 상태에서 순환으로 제한됩니다(Auffray et al., 2007; Carlin et al., 2013; Collison et al., 2015). 정상 상태에서 중간 단핵구의 역할에 대한 증거는 여전히 부족하지만 이들 세포는 다른 하위 집합과 비교하여 가장 높은 수준의 HLA-DR을 발현하며(Patel et al., 2017) 이는 항원 제시에서 잠재적인 역할을 시사합니다. 최근 중간 단핵구는 두 개의 이질적인 집단으로 구성되는 것으로 제안되었지만(Villani et al., 2017), 이들의 역할을 확인하려면 추가 실험이 필요합니다.
염증에서 단핵구의 역할
감염이나 손상에 반응하여 전형적인 단핵구는 염증 부위로 모집됩니다(Geissmann, Jung 및 Littman, 2003; Nahrendorf et al., 2007; Tsou et al., 2007). 케모카인 수용체인 CCR2는 골수 유출에 필요하므로 순환하는 고전적 단핵구가 부족한 CCR2-\- 마우스를 사용하여 조직 손상/감염에 대한 기여를 연구했습니다. 고전적 단핵구는 염증성 단핵구로 언급되었지만, 비고전적 단핵구는 류마티스 관절염의 쥐 모델과 같은 일부 병리와도 관련되어 있습니다(Misharin et al., 2014).
급성 국소 염증의 인간 모델에서 고전적인 단핵구는 초기 시점에서 관찰되었고 중간 단핵구 표현형은 후기 사건에서 관찰되었지만(Motwani et al., 2016), 중간 단핵구가 순환 풀에서 유래되었는지 또는 그들은 현장의 고전적인 단핵구로부터 성숙되었습니다. 단핵구 유래 세포는 대식세포와 유사한 기능을 나타내거나 수지상 세포처럼 행동할 수 있습니다. 최근에는 특정 전사 인자와 아릴 탄화수소 수용체의 결찰이 단핵구 유래 세포의 운명을 결정하는 데 관여하는 것으로 나타났습니다(Goudot et al., 2017).
모집된 단핵구가 장기 조직 대식세포에 기여하는지 여부도 조사 분야입니다. 일부 연구에서는 챌린지 후 단핵구가 조직에 지속된다고 보고했지만(Yona et al., 2013; Machiels et al., 2017), 다른 조건에서는 단핵구 유래 세포가 세포사멸에 의해 해결되는 동안 제거되는 것으로 나타났습니다. (Janssen et al., 2011).
요약
요약하면, 단핵 식세포는 면역 체계뿐만 아니라 생리학적 항상성을 유지하는 데에도 중요한 역할을 합니다. 이러한 세포의 중요성은 발달에 필요한 전사 인자의 돌연변이로 인해 순환 단핵 식세포가 결핍된 환자에게 강조될 수 있습니다(Bigley et al., 2011; Dickinson et al., 2011; Hambleton et al., 2011; Frankenberger 등, 2013). 건강과 질병 모두에서 단핵 식세포 사이의 역할과 관계를 평가하는 연구가 계속 진행되고 있습니다. 더 명확하게 이해하면 이러한 세포가 필요할 때 유익한 기능을 증가시키거나 해로운 환경에서 기능적 용량을 감소시키는 것을 목표로 할 수 있기를 바랍니다.
참고자료
Auffray, C., Fogg, D., Garfa, M., Elain, G., Join-Lambert, O., Kayal, S., Sarnacki, S., Cumano, A., Lauvau, G. 및 Geissmann, F (2007) '순찰 행동을 보이는 단핵구 집단에 의한 혈관 및 조직 모니터링.', Science(New York, N.Y.), 317(5838), pp. 666-70. 도이: 10.1126/science.1142883.
Bain, C. C., Bravo-Blas, A., Scott, C. L., Perdiguero, E. G., Geissmann, F., Henri, S., Malissen, B., Osborne, L. C., Artis, D. 및 Mowat, A. M. (2014) 순환하는 단핵구로부터의 지속적인 보충은 성체 쥐의 장에서 대식세포 풀을 유지합니다.', Nature Immunology, (8월). 도이: 10.1038/ni.2967.
Barth, M. W., Hendrzak, J. A., Melnicoff, M. J. 및 Morahan, PS (1995) '대식세포 소멸 반응에 대한 검토.', Journal of leukocyte Biology, 57(3), pp. 361-7. 이용 가능: http://www.jleukbio.org/content/57/3/361.abstract...
Bedoui, S., Whitney, P. G., Waithman, J., Eidsmo, L., Wakim, L., Caminschi, I., Allan, R. S., Wojtasiak, M., Shortman, K., Carbone, F. R., Brooks, A. G. 및 Heath, W. R. (2009) '피부 유래 CD103+ 수지상 세포에 의한 바이러스 및 자가 항원의 교차 제시.', Nature Immunology, 10(5), pp. 488-495. 도이: 10.1038/ni.1724.
Bigley, V., Haniffa, M., Doulatov, S., Wang, X.-N., Dickinson, R., McGovern, N., Jardine, L., Pagan, S., Dimmick, I., Chua, I., Wallis, J., Lordan, J., Morgan, C., Kumararatne, D. S., Doffinger, R., van der Burg, M., van Dongen, J., Cant, A., Dick, J. E., Hambleton , S. 및 Collin, M. (2011) '인간 수지상 세포, 단핵구, B 및 NK 림프성 결핍 증후군.', The Journal of Experiment Medicine, 208(2), pp. 227–234. 도이: 10.1084/jem.20101459.
Carlin, L. M., Stamatiades, E. G., Auffray, C., Hanna, R. N., Glover, L., Vizcay-Barrena, G., Hedrick, C. C., Cook, H. T., Diebold, S. 및 Geissmann, F. (2013) Nr4a1 의존성 Ly6Clow 단핵구는 내피 세포를 모니터링하고 이들의 처리를 조율합니다', Cell, 153(2), pp. 362–375. 도이: 10.1016/j.cell.2013.03.010.
Cisse, B., Caton, M. L., Lehner, M., Maeda, T., Scheu, S., Locksley, R., Holmberg, D., Zweier, C., den Hollander, N. S., Kant, S. G., Holter, W., Rauch, A., Zhuang, Y. 및 Reizis, B. (2008) '전사 인자 E2-2는 형질세포성 수지상 세포 발달의 필수적이고 구체적인 조절자입니다', Cell, 135(1), pp. 37– 48. 도이: 10.1016/j.cell.2008.09.016.
Cline, M. J. 및 Moore, M. A. (1972) 'Embryonic Origin of the mouse Macrophage.', Blood, 39(6), pp. 842-9. 이용 가능: http://www.ncbi.nlm.nih.gov/pubmed/5028525.
Collison, J. L., Carlin, L. M., Eichmann, M., Geissmann, F. 및 Peakman, M. (2015) '시험관 내 인간 혈관 내피 세포에 대한 인간 단핵구 하위 집합의 이동 행동의 이질성.', 면역학 저널(볼티모어, 메릴랜드: 1950), 195(3), pp. 1162–70. 도이: 10.4049/jimunol.1401806.
Dickinson, R. E., Griffin, H., Bigley, V., Reynard, L. N., Hussain, R., Haniffa, M., Lakey, J. H., Rahman, T., Wang, X. N., McGovern, N., Pagan, S. , Cookson, S., McDonald, D., Chua, I., Wallis, J., Cant, A., Wright, M., Keavney, B., Chinnery, P. F., Loughlin, J., Hambleton, S., Santibanez-Koref, M. 및 Collin, M. (2011) 'Exome 염기서열 분석을 통해 GATA-2 돌연변이가 수지상 세포, 단핵구, B 및 NK 림프 결핍의 원인임을 확인합니다.', Blood, 118(10), pp. 2656–2658 . 도이: 10.1182/blood-2011-06-360313.
Ebert, R. H. 및 Florey, H. W. (1939) '생체 내에서 관찰된 단핵구의 혈관 외 발달', British Journal of Experimental Pathology, 20(1), p. 342. 이용 가능: http://www.ncbi.nlm.nih.gov/pubmed/2065374%5Cnhtt...
Epelman, S., Lavine, K. J., Beaudin, A. E., Sojka, D. K., Carrero, J. A., Calderon, B., Brija, T., Gautier, E. L., Ivanov, S., Satpathy, A. T., Schilling, J. D., Schwendener, R., Sergin, I., Razani, B., Forsberg, E. C., Yokoyama, W. M., Unanue, E. R., Colonna, M., Randolph, G. J. 및 Mann, D. L. (2014) '배아 및 성인 유래 상주 심장 대식세포는 정상 상태와 염증 중에 뚜렷한 메커니즘을 통해 유지됩니다.', 면역. Elsevier Inc., 40(1), pp. 91–104. 도이: 10.1016/j.immuni.2013.11.019
Frankenberger, M., Ekici, A. B., Angstwurm, M. W., Hoffmann, H., Hofer, T. P. J., Heimbeck, I., Meyer, P., Lohse, P., Wjst, M., Häussinger, K., Reis, A 및 Ziegler-Heitbrock, L. (2013) 'CD16 양성 단핵구의 결함은 질병 없이 발생할 수 있습니다', 면역생물학. Elsevier GmbH., 218(2), pp. 169–174. 도이: 10.1016/j.imbio.2012.02.013.
van Furth, R., Cohn, Z. A., Hirsch, J. G., Humphrey, J. H., Spector, W. G. 및 Langevoort, H. L. (1972) '단핵 식세포 시스템: 대식세포, 단핵구 및 이들의 전구체 세포의 새로운 분류.', 게시판 세계보건기구, 46, pp. 845-852.
Gamrekelashvili, J., Giagnorio, R., Jussofie, J., Soehnlein, O., Duchene, J., Briseño, C. G., Ramasamy, S. K., Krishnasamy, K., Limbourg, A., Kapanadze, T., Ishifune, C., Hinkel, R., Radtke, F., Strobl, L. J., Zimber-Strobl, U., Napp, L. C., Bauersachs, J., Haller, H., Yasutomo, K., Kupatt, C., Murphy, K. M., Adams, R. H., Weber, C. 및 Limbourg, F. P. (2016) 'Notch 신호 전달에 의해 매개되는 혈관에 의한 단핵구 세포 운명의 조절', Nature communications, 7, p. 12597. doi: 10.1038/ncomms12597.
Geissmann, F., Jung, S. 및 Littman, D. R. (2003) '혈액 단핵구는 뚜렷한 이동 특성을 지닌 두 가지 주요 하위 집합으로 구성됩니다', Immunity, 19(1), pp. 71-82. 도이: 10.1016/S1074-7613(03)00174-2.
Ginhoux, F., Greter, M., Leboeuf, M., Nandi, S., See, P., Gokhan, S., Mehler, M. F., Conway, S. J., Ng, L. G., Stanley, E. R., Samokhvalov, I. M. 및 Merad, M. (2010) '운명 지도 분석에 따르면 성체 소교세포는 원시 대식세포에서 유래한 것으로 나타났습니다.', Science(New York, N.Y.), 330(6005), pp. 841–5. 도이: 10.1126/science.1194637.
Goudot, C., Coillard, A., Villani, A.-C., Gueguen, P., Cros, A., Sarkizova, S., Tang-Huau, T.-L., Bohec, M., Baulande, S., Hacohen, N., Amigorena, S. 및 Segura, E. (2017) '아릴 탄화수소 수용체는 단핵구의 수지상 세포 대 대식세포로의 분화를 제어합니다', Immunity, 47(3), p. 582–596.e6. 도이: 10.1016/j.immuni.2017.08.016.
Guilliams, M., De Kleer, I., Henri, S., Post, S., Vanhoutte, L., De Prijck, S., Deswarte, K., Malissen, B., Hammad, H. 및 Lambrecht, B. N. (2013) '폐포 대식세포는 GM-CSF를 통해 생후 첫 주에 수명이 긴 세포로 분화하는 태아 단핵구에서 발생합니다.', The Journal of Experiment Medicine, 210(10), pp. 1977-92. 도이: 10.1084/jem.20131199.
Guilliams, M. 및 Scott, C. L. (2017) '틈새 경쟁이 조직 상주 대식세포의 기원을 결정합니까?', Nature Reviews Immunology, 17(7), pp. 451-460. 도이: 10.1038/nri.2017.42.
den Haan, J. M., Lehar, S. M. 및 Bevan, M. J. (2000) 'CD8(+)이지만 CD8(-)이 아닌 수지상 세포는 in vivo에서 교차 프라임 세포독성 T 세포.', The Journal of Experiment Medicine, 192(12), 1685~96페이지. 도이: 10.1084/jem.192.12.1685.
Hambleton, S., Salem, S., Bustamante, J., Bigley, V., Boisson-Dupuis, S., Azevedo, J., Fortin, A., Haniffa, M., Ceron-Gutierrez, L., 베이컨 , C. M., Menon, G., Trouillet, C., McDonald, D., Carey, P., Ginhoux, F., Alsina, L., Zumwalt, T. J., Kong, X.-F., Kumararatne, D., Butler, K., Hubeau, M., Feinberg, J., Al-Muhsen, S., Cant, A., Abel, L., Chaussabel, D., Doffinger, R., Talesnik, E., Grumach, A ., Duarte, A., Abarca, K., Moraes-Vasconcelos, D., Burk, D., Berghuis, A., Geissmann, F., Collin, M., Casanova, J.-L. 및 Gros, P. (2011) 'IRF8 돌연변이 및 인간 수지상 세포 면역결핍', New England Journal of Medicine, 365(2), pp. 127-138. 도이: 10.1056/NEJMoa1100066.
Hashimoto, D., Chow, A., Noizat, C., Teo, P., Beasley, M. B., Leboeuf, M., Becker, C. D., See, P., Price, J., Lucas, D., Greter, M., Mortha, A., Boyer, S. W., Forsberg, E. C., Tanaka, M., van Rooijen, N., García-Sastre, A., Stanley, E. R., Ginhoux, F., Frenette, P. S. 및 Merad, M (2013) '조직 상주 대식세포는 순환 단핵구의 기여를 최소화하면서 성인 생활 전반에 걸쳐 국소적으로 자가 유지됩니다', 면역, 38(4), pp. 792-804. 도이: 10.1016/j.immuni.2013.04.004.
Hoeffel, G., Wang, Y., Greter, M., See, P., Teo, P., Malleret, B., Leboeuf, M., Low, D., Oller, G., Almeida, F., Choy, S. H. Y., Grisotto, M., Renia, L., Conway, S. J., Stanley, E. R., Chan, J. K. Y., Ng, L. G., Samokhvalov, I. M., Merad, M. 및 Ginhoux, F. (2012) '성인 랑게르한스 세포 주로 배아 태아 간 단핵구에서 유래하며 난황낭 유래 대식세포가 약간 기여합니다.', The Journal of Experiment Medicine, 209(6), pp. 1167-81. 도이: 10.1084/jem.20120340.
Jakubzick, C., Gautier, E. L., Gibbings, S. L., Sojka, D. K., Schlitzer, A., Johnson, T. E., Ivanov, S., Duan, Q., Bala, S., Condon, T., van Rooijen, N ., Grainger, J. R., Belkaid, Y., Ma'ayan, A., Riches, D. W. H., Yokoyama, W. M., Ginhoux, F., Henson, P. M. 및 Randolph, G. J. (2013) '조사에 따른 고전 단핵구의 최소 분화 항정상태 조직과 항원을 림프절로 수송합니다.', 면역. Elsevier Inc., 39(3), 599-610페이지. 도이: 10.1016/j.immuni.2013.08.007.
Janssen, W. J., Barthel, L., Muldrow, A., Oberley-Deegan, R. E., Kearns, M. T., Jakubzick, C. 및 Henson, P. M. (2011) 'Fas는 급성 폐의 해결 중에 상주 및 모집된 대식세포의 차등 운명을 결정합니다. 부상', 미국 호흡기 및 중환자 치료 의학 저널, 184(5), pp. 547–560. doi: 10.1164/rccm.201011-1891OC.
Jenkins, S. J., Ruckerl, D., Cook, P. C., Jones, L. H., Finkelman, F. D., van Rooijen, N., MacDonald, A. S. 및 Allen, J. E. (2011) '혈액 모집보다는 국소 대식세포 증식이 TH2 염증의 서명', Science, 332(6035), pp. 1284–1288. 도이: 10.1126/science.1204351.
Jung, S., Unutmaz, D., Wong, P., Sano, G. I., De Los Santos, K., Sparwasser, T., Wu, S., Vuthoori, S., Ko, K., Zavala, F. , Pamer, E. G., Littman, D. R. 및 Lang, R. A. (2002) 'CD11c+ 수지상 세포의 생체 내 고갈은 외인성 세포 관련 항원에 의한 CD8+ T 세포의 프라이밍을 폐지합니다', Immunity, 17(2), pp. 211–220. 도이: 10.1016/S1074-7613(02)00365-5.
Keller, N. M., Gentek, R., Gimenez, G., Bigot, S., Mailfert, S. 및 Sieweke, M. H. (2017) '뚜렷한 고환 대식세포 집단의 발달 기원 및 유지', Jem, 214(10), pp .1–14. 도이: 10.1084/jem.20170829.
Kohyama, M., Ise, W., Edelson, B. T., Wilker, P. R., Hildner, K., Mejia, C., Frazier, W. a, Murphy, T. L. 및 Murphy, K. M. (2009) 'Spi-C의 역할 적색속 대식세포 및 비장 철 항상성의 발달에.', Nature. Nature Publishing Group, 457(7227), pp. 318–21. 도이: 10.1038/nature07472.
Lavin, Y., Winter, D., Blecher-Gonen, R., David, E., Keren-Shaul, H., Merad, M., Jung, S. 및 Amit, I. (2014) '조직 레지던트 대식세포 강화제 풍경은 지역 미세환경'인 Cell에 의해 형성됩니다. Elsevier Inc., 159(6), pp. 1312–1326. 도이: 10.1016/j.cell.2014.11.018.
Leid, J., Carrelha, J., Boukarabila, H., Epelman, S., Jacobsen, S. E. W. 및 Lavine, K. J. (2016) '관상동맥 발달 및 성숙에 원시 배아 대식세포가 필요합니다', 순환 연구, 118(10) , pp. 1498–1511. 도이: 10.1161/CIRCRESAHA.115.308270.
Machiels, B., Dourcy, M., Xiao, X., Javaux, J., Mesnil, C., Sabatel, C., Desmecht, D., Lallemand, F., Martinive, P., Hammad, H., Guilliams, M., Dewals, B., Vanderplasschen, A., Lambrecht, B. N., Bureau, F. 및 Gillet, L. (2017) '감마헤르페스바이러스는 상주하는 폐포 대식세포를 조절 단핵구로 대체하도록 유도하여 알레르기성 천식에 대한 보호를 제공합니다. ', 자연면역학. 네이처출판그룹(10월). 도이: 10.1038/ni.3857.
Mass, E., Ballesteros, I., Farlik, M., Halbritter, F., Günther, P., Crozet, L., Jacome-Galarza, C. E., Händler, K., Klughammer, J., Kobayashi, Y. , Gomez-Perdiguero, E., Schultze, J. L., Beyer, M., Bock, C. 및 Geissmann, F. (2016) '기관 형성 중 조직 상주 대식세포의 사양.', Science(New York, NY), 353 (6304). 도이: 10.1126/science.aaf4238.
McGovern, N., Schlitzer, A., Gunawan, M., Jardine, L., Shin, A., Poyner, E., Green, K., Dickinson, R., Wang, X.-N., Low, D., Best, K., Covins, S., Milne, P., Pagan, S., Aljefri, K., Windebank, M., Miranda-Saavedra, D., Saavedra, D. M., Larbi, A., Wasan , P. S., Duan, K., Poidinger, M., Bigley, V., Ginhoux, F., Collin, M. 및 Haniffa, M. (2014) '인간 진피 CD14+ 세포는 단핵구 유래 대식세포의 일시적인 집단입니다. ', 면역력. 저자, 41(3), 465-77페이지. 도이: 10.1016/j.immuni.2014.08.006.
Mildner, A., Schönheit, J., Giladi, A., David, E., Lara-Astiaso, D., Lorenzo-Vivas, E., Paul, F., Chappell-Maor, L., Priller, J. , Leutz, A., Amit, I. 및 Jung, S. (2017) '쥐과 단핵구의 게놈 특성화는 Ly6C − 세포의 C/EBPβ 전사 인자 의존성을 드러냅니다', Immunity, 46(5), p. 849–862.e7. 도이: 10.1016/j.immuni.2017.04.018.
Minutti, C. M., Jackson-Jones, L. H., García-Fojeda, B., Knipper, J. A., Sutherland, T. E., Logan, N., Rinqvist, E., Guilmat-Prats, R., Ferenbach, D. A., Artigas, A. , Stamme, C., Chroneos, Z. C., Zaiss, D. M., Casals, C. 및 Allen, J. E. (2017) 'IL-4Rα 매개 대식세포 활성화의 국소 증폭기는 폐와 간 회복을 촉진합니다.', Science(New York, N.Y.), 356(6342), pp. 1076–1080. 도이: 10.1126/science.aaj2067.
Misharin, A. V., Cuda, C. M., Saber, R., Turner, J. D., Gierut, A. K., Kenneth Haines, G. K., Berdnikovs, S., Filer, A., Clark, A. R., Buckley, C. D., Mutlu, G. M., Scott Budinger , G. R. 및 Perlman, H. (2014) '비고전적 Ly6C-단핵구는 생쥐에서 염증성 관절염의 발생을 촉진합니다', Cell Reports, 9(2), pp. 591-604. 도이: 10.1016/j.celrep.2014.09.032.
Motwani, M. P., Flint, J. D., Ph, R., Maeyer, D., Fullerton, J. N., Smith, A. M., Marks, D. J. 및 Gilroy, D. W. (2016) 'UV로 죽은 E. coli', Journal of Pathology: Clinical Research, 2(7월), pp. 154–165. 도이: 10.1002/cjp2.43.
Nahrendorf, M., Swirski, F. K., Aikawa, E., Stangenberg, L., Wurdinger, T., Figueiredo, J.-L., Libby, P., Weissleder, R. 및 Pittet, M. J. (2007) 심근 치유는 서로 다른 보완적 기능을 가진 두 개의 단핵구 하위 집합을 순차적으로 동원합니다.', The Journal of Experiment Medicine, 204(12), pp. 3037–47. 도이: 10.1084/jem.20070885.
Nussenzweig, M. C., Steinman, R. M., Gutchinov, B. 및 Cohn, Z. A. (1980) '수지상 세포는 항트리니트로페닐 세포독성 T 림프구의 발달을 위한 보조 세포입니다.', The Journal of Experiment Medicine, 152(4), pp .1070–84. 이용 가능: http://www.ncbi.nlm.nih.gov/pubmed/6968335%5Cnhtt...
Paolicelli, R. C., Bolasco, G., Pagani, F., Maggi, L., Scianni, M., Panzanelli, P., Giustetto, M., Ferreira, T. A., Guiducci, E., Dumas, L., Ragozzino, D. 및 Gross, C. T. (2011) '소교세포에 의한 시냅스 가지치기는 정상적인 뇌 발달에 필요합니다.', Science (New York, N.Y.), 333(6048), pp. 1456–8. 도이: 10.1126/science.1202529.
Parkhurst, C. N., Yang, G., Ninan, I., Savas, J. N., Yates, J. R., Lafaille, J. J., Hempstead, B. L., Littman, D. R. 및 Gan, W. B. (2013) '미크로글리아는 뇌를 통해 학습 의존적 시냅스 형성을 촉진합니다 -유래 신경 영양 인자', Cell, 155(7), pp. 1596–1609. 도이: 10.1016/j.cell.2013.11.030.
Patel, A. A., Zhang, Y., Fullerton, J. N., Boelen, L., Rongvaux, A., Maini, A. A., Bigley, V., Flavell, R. A., Gilroy, D. W., Asquith, B., Macallan, D. 및 Yona, S. (2017) '정상 상태 및 전신 염증에서 인간 단핵구 하위 집합의 운명과 수명', The Journal of Experimental Medicine, 214(7), pp. 1913-1923. 도이: 10.1084/jem.20170355.
Schulz, C., Gomez Perdiguero, E., Chorro, L., Szabo-Rogers, H., Cagnard, N., Kierdorf, K., Prinz, M., Wu, B., Jacobsen, S. E. W., Pollard, J. W. , Frampton, J., Liu, K. J. 및 Geissmann, F. (2012) 'Myb 및 조혈 줄기 세포와 무관한 골수 세포 계통.', Science (New York, NY), 336, pp. 86–90. 도이: 10.1126/science.1219179.
P., Dutertre, C.-A., Chen, J., Günther, P., McGovern, N., Irac, S. E., Gunawan, M., Beyer, M., Händler, K., Duan, K 참조 ., Sumatoh, H. R. Bin, Ruffin, N., Jouve, M., Gea-Mallorquí, E., Hennekam, R. C. M., Lim, T., Yip, C. C., Wen, M., Malleret, B., Low, I ., Shadan, N. B., Fen, C. F. S., Tay, A., Lum, J., Zolezzi, F., Larbi, A., Poidinger, M., Chan, J. K. Y., Chen, Q., Rénia, L., Haniffa , M., Benaroch, P., Schlitzer, A., Schultze, J. L., Newell, E. W. 및 Ginhoux, F. (2017) '고차원 기술의 통합을 통해 인간 DC 계보 매핑', Science, 356(6342) ), p. eaag3009. 도이: 10.1126/science.aag3009.
Soucie, E. L., Soucie, E. L., Weng, Z., Geirsdóttir, L., Molawi, K., Maurizio, J., Fenouil, R., Mossadegh-keller, N., Gimenez, G., Vanhille, L., Favret, J., Berruyer, C., Perrin, P., Hacohen, N., Andrau, J., Dubreuil, P., Sidow, A. 및 Sieweke, M. H. (2016) '리니지 특이적 강화제는 자가 갱신을 활성화합니다 대식세포 및 배아줄기세포의 유전자', 5510, pp. 1-20. 도이: 10.1126/science.aad5510.
Steinman, R. M. 및 Cohn, Z. a (1973) '생쥐의 말초 림프 기관에서 새로운 세포 유형의 확인. I. 형태학, 정량화, 조직 분포.', The Journal of Experiment Medicine, 137(5), pp. 1142-1162. 도이: 10.1084/jem.137.5.1142.
Takahashi, K. (1989) '마우스 난황낭의 분화, 성숙 및 증식 대식세포: 및 초미세구조 연구', Journal of Leukocyte Biology, 96(2), pp. 87-96.
Tsou, C. L., Peters, W., Si, Y., Slaymaker, S., Aslanian, A. M., Weisberg, S. P., Mack, M. 및 Charo, I. F. (2007) '단핵구 동원에서 CCR2 및 MCP-3의 중요한 역할 골수 및 염증 부위 모집에서 ', Journal of Clinical Investigation, 117(4), pp. 902-909. 도이: 10.1172/JCI29919.
van de Laar, L., Saelens, W., De Prijck, S., Martens, L., Scott, C. L., Van Isterdael, G., Hoffmann, E., Beyaert, R., Saeys, Y., Lambrecht, B. N. 및 Guilliams, M. (2016) '난황낭 대식세포, 태아 간 및 성체 단핵구는 빈 틈새에 정착하여 기능성 조직 상주 대식세포로 발전할 수 있습니다', 면역. Elsevier Inc., 1~14페이지. 도이: 10.1016/j.immuni.2016.02.017.
Varol, C., Landsman, L., Fogg, D. K., Greenshtein, L., Gildor, B., Margalit, R., Kalchenko, V., Geissmann, F. 및 Jung, S. (2007) '단핵구는 비장이 아닌 점막의 기존 수지상 세포에 발생합니다.', The Journal of Experiment Medicine, 204(1), pp. 171-80. 도이: 10.1084/jem.20061011.
Villani, A.-C., Satija, R., Reynolds, G., Sarkizova, S., Shekhar, K., Fletcher, J., Griesbeck, M., Butler, A., Zheng, S., Lazo, S., Jardine, L., Dixon, D., Stephenson, E., Nilsson, E., Grundberg, I., McDonald, D., Filby, A., Li, W., De Jager, P. L., Rozenblatt- Rosen, O., Lane, A. A., Haniffa, M., Regev, A. 및 Hacohen, N. (2017) '단일 세포 RNA-seq는 새로운 유형의 인간 혈액 수지상 세포, 단핵구 및 전구 세포를 드러냅니다', Science, 356(6335), p. 에아아4573. 도이: 10.1126/science.aah4573.
Yamasaki, R., Lu, H., Butovsky, O., Ohno, N., Rietsch, A. M., Cialic, R., Wu, P. M., Doykan, C. E., Lin, J., Cotleur, A. C., Kidd, G. , Zorlu, M. M., Sun, N., Hu, W., Liu, L., Lee, J.-C., Taylor, S. E., Uehlein, L., Dixon, D., Gu, J., Floruta, C. M. , Zhu, M., Charo, I. F., Weiner, H. L. 및 Ransohoff, R. M. (2014) '염증이 있는 중추 신경계에서 미세아교세포와 단핵구의 다른 역할', The Journal of Experimental Medicine, 211(8), pp. 1533– 1549. 도이: 10.1084/jem.20132477.
Yona, S., Kim, K. W., Wolf, Y., Mildner, A., Varol, D., Breker, M., Strauss-Ayali, D., Viukov, S., Guilliams, M., Misharin, A. , Hume, D. A., Perlman, H., Malissen, B., Zelzer, E. 및 Jung, S. (2013) '운명 매핑은 항상성 하에서 단핵구와 조직 대식세포의 기원과 역학을 드러냅니다', 면역, 38, pp. 79 -91. 도이: 10.1016/j.immuni.2012.12.001.
Ziegler-Heitbrock, L. (2014) '인간 및 기타 종의 단핵구 하위 집합', 세포 면역학. Elsevier Inc., 289(1–2), pp. 135–139. 도이: 10.1016/j.cellimm.2014.03.019.
19th Aug 2024
Recent Posts
-
슈반 세포: 신경 기능을 지원하는 특수 세포
슈반 세포는 신경 기능에 중요한 역할을 하는 세포입니다. 그들은 축삭을 수초화하고 뉴런 사이의 전기 신호 전달을 보장하는 역할을 담당합니다. 슈반 세포는 …25th Sep 2024 -
신경면역학: CNS의 면역체계
신경면역학이란 무엇입니까?신경면역학은 중추신경계(CNS)와 면역체계 사이의 복잡하고 양방향 상호작용을 조사하는 데 전념하는 다학제적 과학 분야입니다. 여기 …25th Sep 2024 -
바르덴부르크 증후군 및 클라인-바르덴부르크 증후군
바르덴부르크 증후군: 색소 침착, 청력 등에 영향을 미치는 희귀 유전 질환바르덴부르크 증후군(WS)은 개인의 외모와 감각 능력의 다양한 측면에 영향을 미치 …25th Sep 2024