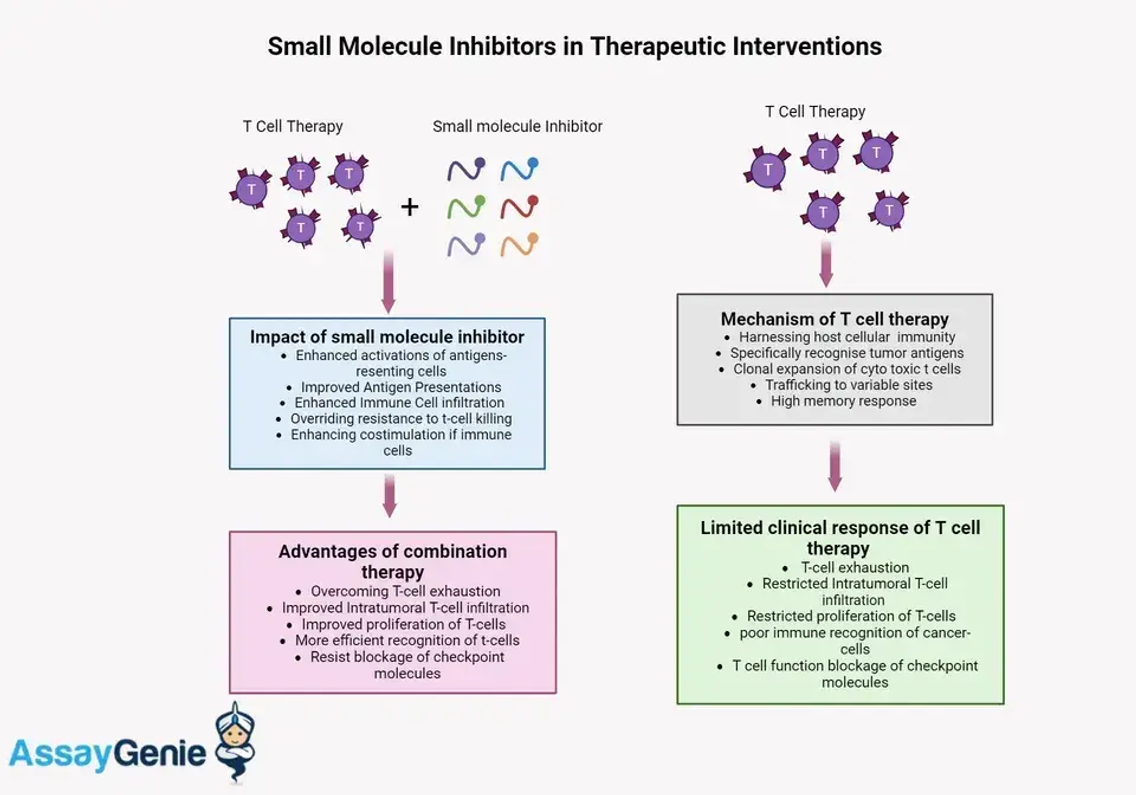
치료 중재에서 소분자 억제제의 장점
소분자 억제제는 암, 바이러스 감염, 만성 염증성 질환을 포함한 수많은 질병을 치료하기 위한 다재다능한 접근 방식을 제공함으로써 치료 개입 분야에서 상당한 발전을 보여줍니다. 일반적으로 900 달톤 미만의 분자량을 갖는 이러한 화합물은 세포 내의 특정 단백질 표적과 상호 작용하여 생물학적 과정을 조절할 수 있습니다. 이 기사에서는 소분자 억제제의 다각적인 장점을 탐구하고 표적 치료법 개발에서 역할을 강조합니다.
표적 특이성 및 선택성:
소분자 억제제의 가장 큰 장점 중 하나는 질병 병리와 관련된 특정 단백질이나 효소를 선택적으로 표적으로 삼는 능력입니다. 이러한 특이성은 건강한 세포에 대한 영향을 최소화하여 기존 화학요법제에서 흔히 볼 수 있는 표적 외 효과 및 관련 독성의 위험을 줄입니다. 소분자 억제제는 암의 티로신 키나제와 같이 질병 진행에 중요한 분자에 초점을 맞춤으로써 매우 정밀하게 질병 경로를 효과적으로 방해할 수 있습니다.
경구 생체 이용률 및 투여:
이러한 억제제는 작은 크기와 화학적 특성으로 인해 경구 생체 이용률이 가능하므로 더 큰 규모의 생물학적 치료제에 필요한 정맥 내 또는 피하 투여 방법에 비해 환자에게 더 편리합니다. 경구 투여는 환자 순응도를 향상시킬 뿐만 아니라 만성 질환에서 치료 약물 수준을 유지하는 데 중요한 지속적인 일일 투여를 가능하게 합니다.
침투 및 배포:
소분자 억제제는 조직에 쉽게 침투하고 혈액뇌관문(BBB)을 포함한 세포 장벽을 통과할 수 있습니다. 이 능력은 뇌로의 효과적인 약물 전달이 종종 중요한 과제인 중추신경계(CNS) 장애 및 암 치료에 특히 유용합니다. 작은 크기와 친유성 특성을 통해 이러한 분자는 더 큰 생물학적 치료법으로는 접근할 수 없는 세포내 표적에 도달할 수 있습니다.
약물 설계의 유연성:
비용 효율성:
생물학적 치료법에 비해 소분자 억제제는 일반적으로 제조 및 유통 비용이 저렴합니다. 이러한 비용 효율성 덕분에 특히 의료 자원이 제한적일 수 있는 저소득 및 중간 소득 국가에서 더 넓은 환자 집단이 더 쉽게 접근할 수 있습니다. 더욱이, 더 낮은 비용은 더 넓은 보험 적용 범위와 환급으로 이어질 수 있으며, 이러한 치료법에 대한 환자 접근성을 더욱 향상시킬 수 있습니다.
신속한 개발 및 승인 프로세스:
저분자 약물의 개발 주기는 일반적으로 생물학적 제제의 개발 주기보다 짧습니다. 효능과 독성에 대한 높은 처리량 스크리닝을 수행하는 능력과 함께 잘 이해된 제조 공정을 통해 약물 발견 및 개발 일정을 가속화할 수 있습니다. 이러한 신속한 개발 경로는 더 빠른 규제 승인으로 이어져 환자를 위한 새로운 치료법에 대한 시기적절한 접근을 보장할 수 있습니다.
결론
소분자 억제제는 다양한 질병에 걸쳐 표적화되고 효율적이며 비용 효과적인 치료 옵션을 제공하여 치료 개입의 환경에 혁명을 일으켰습니다. 질병 관련 단백질을 선택적으로 방해하는 능력은 유리한 약동학적 특성 및 투여 용이성과 결합되어 현대 의학에서 중요한 역할을 강조합니다. 연구 개발이 계속 발전함에 따라 충족되지 않은 의학적 요구를 충족할 수 있는 소분자 억제제의 잠재력은 여전히 유망하며 차세대 치료법을 위한 길을 닦고 있습니다.
참고자료
Bedard, P. L., Hyman, D. M., Davids, M. S., & Siu, L. L. (2020). 작은 분자, 큰 영향: 종양학 분야의 20년 표적 치료. 랜싯, 395(10229), 1078-1088.
Rozpedek, W., Nowak, A., Pytel, D., Alan Diehl, J., & Majsterek, I. (2017). ER 스트레스 유발 신호 전달 경로의 소분자 억제제를 기반으로 한 인간 질병 및 표적 치료의 분자 기반. 현행분자의학, 17(2), 118-132.
Arkin, M.R., & Wells, J.A.(2004). 단백질-단백질 상호작용의 소분자 억제제: 꿈을 향해 나아가고 있습니다. Nature review Drug discovery, 3(4), 301-317.
Wilson, D. M., & Simeonov, A. (2010). APE1의 DNA 복구 뉴클레아제 활성에 대한 소분자 억제제. 세포 및 분자 생명 과학, 67, 3621-3631.
추이, J.J.(2014). 암에서의 수용체 티로신 키나제 MET 표적화: 소분자 억제제 및 임상 진행. 의약화학저널, 57(11), 4427-4453.
17th Jul 2024
Recent Posts
-
슈반 세포: 신경 기능을 지원하는 특수 세포
슈반 세포는 신경 기능에 중요한 역할을 하는 세포입니다. 그들은 축삭을 수초화하고 뉴런 사이의 전기 신호 전달을 보장하는 역할을 담당합니다. 슈반 세포는 …25th Sep 2024 -
신경면역학: CNS의 면역체계
신경면역학이란 무엇입니까?신경면역학은 중추신경계(CNS)와 면역체계 사이의 복잡하고 양방향 상호작용을 조사하는 데 전념하는 다학제적 과학 분야입니다. 여기 …25th Sep 2024 -
바르덴부르크 증후군 및 클라인-바르덴부르크 증후군
바르덴부르크 증후군: 색소 침착, 청력 등에 영향을 미치는 희귀 유전 질환바르덴부르크 증후군(WS)은 개인의 외모와 감각 능력의 다양한 측면에 영향을 미치 …25th Sep 2024